สารละลายคือส่วนผสมที่เป็นเนื้อเดียวกันซึ่งประกอบด้วยสารตั้งแต่สองชนิดขึ้นไปในขณะที่ความสามารถในการละลายคือปริมาณสูงสุดของสารประกอบหรือสารที่สามารถละลายได้ในตัวทำละลายหลายชนิด
วิธีแก้ปัญหามากมายที่เราพบในชีวิตประจำวัน ได้แก่ น้ำเชื่อมหวานหนึ่งแก้ว ในน้ำเชื่อมหนึ่งแก้วมีส่วนประกอบหลายอย่าง ได้แก่ น้ำน้ำเชื่อมและน้ำตาล
หากส่วนประกอบเหล่านี้ผสมกันจนมองไม่เห็นส่วนประกอบที่เป็นส่วนประกอบอีกต่อไปก็จะกลายเป็นวิธีการแก้
เมื่อพิจารณาถึงวิธีการแก้ปัญหาการทบทวนเพิ่มเติมต่อไปนี้จะรวมถึงนิยามคุณสมบัติประเภทและปัจจัยของโซลูชัน
ความหมายของสารละลายและความสามารถในการละลาย

วิธีการแก้
สารละลายคือส่วนผสมที่เป็นเนื้อเดียวกันซึ่งประกอบด้วยสารตั้งแต่สองชนิดขึ้นไป เรียกว่าโซลูชันเนื่องจากส่วนประกอบที่เป็นส่วนประกอบของโซลูชัน
ในสารละลายมีตัวทำละลายและตัวถูกละลาย ตัวละลาย (Solute) เป็นสารที่ประกอบขึ้นเป็นสารละลายที่มีปริมาณน้อยกว่าในสารละลาย ในขณะเดียวกันตัวทำละลาย (ตัวทำละลาย) เป็นสารที่มีปริมาณมากกว่าตัวถูกละลาย
องค์ประกอบของสารทะเลในสารละลายแสดงโดยความเข้มข้นของสารละลาย ในขณะที่กระบวนการผสมตัวถูกละลายและตัวทำละลายเพื่อสร้างสารละลายเรียกว่าการละลายหรือการละลาย
หากต้องการทำความเข้าใจเพิ่มเติมเกี่ยวกับวิธีแก้ปัญหาให้พิจารณาภาพประกอบต่อไปนี้
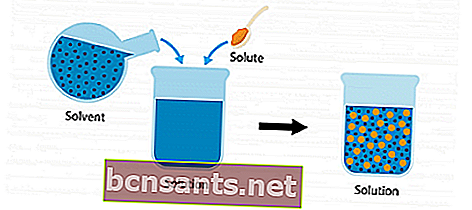
มีตัวถูกละลายและตัวทำละลาย เมื่อส่วนผสมทั้งสองผสมกันและรวมกันในภาชนะจะกลายเป็นสารละลาย
ความสามารถในการละลาย
ความหมายของความสามารถในการละลายคือปริมาณสูงสุดของสารประกอบหรือสารที่สามารถละลายได้ในตัวทำละลายจำนวนหนึ่ง
ความสามารถในการละลายมีสัญลักษณ์โดยs ( ความสามารถในการละลาย) ในหน่วย mol / L หรือโดยปกติจะใช้หน่วยโมลาริตี M นี่คือสูตรสำหรับความสามารถในการละลายหรือโมลาริตี
M = n / V
โดยที่ M คือโมลาริตี (mol / L), n คือจำนวนโมลของสาร (โมล) และ V คือปริมาตรของสารละลายหรือตัวทำละลาย (L)
ความสามารถในการละลายหมายถึงความเข้มข้นของสารที่ยังคงสามารถละลายได้ในตัวทำละลายจำนวนหนึ่ง
ผลิตภัณฑ์คงที่การละลาย (Ksp)
ตัวถูกละลายที่ละลายในตัวทำละลายจะก่อให้เกิดปฏิกิริยาสมดุล การเกิดสมดุลได้รับอิทธิพลจากตัวละลายที่ไม่ละลายน้ำและไอออนของตัวถูกละลาย
อ่านเพิ่มเติม: 100+ ตัวอย่างคำมาตรฐานและคำที่ไม่เป็นมาตรฐาน + คำอธิบาย [อัพเดท]ต่อไปนี้เป็นตัวอย่างของค่าคงที่สมดุลสำหรับปฏิกิริยา
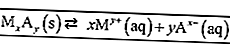
ตามกฎสำหรับการเขียนสูตรสมดุลสารในรูปของสารละลาย (aq) และก๊าซเท่านั้นที่ถูกเขียนลงในสูตร เพื่อให้ได้มา:
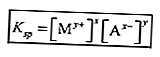
ค่าคงที่สมดุลสำหรับสารละลายที่ละลายได้ยากเรียกว่าค่าคงที่ของผลิตภัณฑ์การละลาย (Ksp)
คุณสมบัติของโซลูชัน

คุณสมบัติทางกายภาพที่ปรากฏในสารละลายแบ่งออกเป็นสามส่วน ได้แก่ :
1. Colligative Properties of Solutions
เป็นลักษณะของสารละลายที่ขึ้นอยู่กับจำนวนอนุภาคของตัวถูกละลายในสารละลายและไม่ขึ้นอยู่กับชนิดของอนุภาคตัวทำละลาย
สมบัติการรวมตัวจะเทียบเท่ากับความเข้มข้นของสารที่ไม่ใช่อิเล็กโทรไลต์ต่างๆในสารละลายโดยไม่คำนึงถึงชนิดหรือคุณสมบัติทางเคมีขององค์ประกอบ
ในการพิจารณาคุณสมบัติการเรียงตัวของสารละลายของแข็งในของเหลวของแข็งจะถูกพิจารณาว่าไม่ระเหยและความดันไอเหนือสารละลายมาจากตัวทำละลายทั้งหมด
คุณสมบัติบางประการของสารละลายคือความดันออสโมติกการลดความดันไอเพิ่มจุดเดือดและจุดเยือกแข็งลดลง
2. คุณสมบัติของสารเติมแต่ง
ในสารละลายคุณสมบัติของสารเติมแต่งคือคุณสมบัติของสารละลายที่ขึ้นอยู่กับอะตอมทั้งหมดในโมเลกุลหรือจำนวนคุณสมบัติที่เป็นส่วนประกอบของสารละลาย
ตัวอย่างคุณสมบัติการเติมแต่งของสารละลายคือน้ำหนักโมเลกุลซึ่งเป็นผลรวมของมวลอะตอม
มวลของส่วนประกอบของสารละลายรวมอยู่ในคุณสมบัติของสารเติมแต่งมวลรวมของสารละลายคือปริมาณของแต่ละองค์ประกอบของสารละลาย ได้แก่ ตัวถูกละลายและตัวทำละลาย
3. ธรรมชาติที่เป็นส่วนประกอบ
ซึ่งรวมถึงลักษณะของสารละลายซึ่งขึ้นอยู่กับอะตอมของโมเลกุล (ขึ้นอยู่กับชนิดของอะตอมและจำนวนอะตอม) คุณสมบัติที่เป็นส่วนประกอบบ่งบอกถึงกฎของสารประกอบเดี่ยวและกลุ่มของโมเลกุลในระบบ
มีคุณสมบัติทางกายภาพหลายประการซึ่งเป็นส่วนเสริมและส่วนประกอบ การหักเหของแสงคุณสมบัติทางไฟฟ้าพื้นผิวและคุณสมบัติระหว่างพื้นผิวซึ่งรวมอยู่ในส่วนประกอบบางอย่างและสารเติมแต่งบางชนิด
ประเภทของโซลูชัน

1. สารละลายไม่อิ่มตัว
สารละลายไม่อิ่มตัวหมายถึงสารละลายที่มีตัวถูกละลายน้อยกว่าที่จำเป็นในการทำสารละลายอิ่มตัว สารละลายไม่อิ่มตัวประกอบด้วยอนุภาคที่ไม่ได้ทำปฏิกิริยากับสารอย่างถูกต้องกล่าวอีกนัยหนึ่งก็คือยังคงสามารถละลายสารได้
สารละลายกล่าวว่าไม่อิ่มตัวเมื่อค่าความเข้มข้นของไอออน <Ksp. ในสารละลายไม่อิ่มตัวจะไม่มีการสะสมของตัวถูกละลาย
อ่านเพิ่มเติม: คำจำกัดความของสารละลายเคมีและประเภทและส่วนประกอบ2. สารละลายอิ่มตัว
สารละลายจะรวมอยู่ในสารละลายอิ่มตัวเมื่อมีความสมดุลระหว่างตัวถูกละลายและตัวทำละลาย ในสารละลายอิ่มตัวอนุภาคจะทำปฏิกิริยากับรีเอเจนต์หรือสัมผัสกับความเข้มข้นสูงสุด
สารละลายจะถูกกล่าวว่าอิ่มตัวถ้าความเข้มข้นของไอออนเท่ากับค่า Ksp ในสภาวะสมดุลนี้ความเร็วของตัวถูกละลายในตัวทำละลายจะเท่ากับอัตราที่มันตกตะกอน นั่นคือความเข้มข้นของสารในสารละลายจะเท่ากัน
3. สารละลายอิ่มตัวสูง
นั่นคือสารละลายที่มีตัวถูกละลายมากกว่าตัวทำละลาย สิ่งนี้ทำให้เกิดมูลค่าผลิตภัณฑ์ของความเข้มข้นของไอออน> Ksp เพื่อให้สารละลายอิ่มตัวและตกตะกอน
ปัจจัยการละลาย

ความสามารถในการละลายของของเหลวแตกต่างกันไป สิ่งนี้ได้รับอิทธิพลจากปัจจัยการละลายหลายประการ นี่คือปัจจัยบางประการของการละลาย
1. อุณหภูมิ
ระดับอุณหภูมิของสารละลายมีผลต่อกระบวนการละลายตัวถูกละลาย ที่อุณหภูมิสูงขึ้นตัวถูกละลายจะละลายในตัวทำละลายได้ง่าย
สิ่งนี้เกิดขึ้นเนื่องจากอนุภาคของแข็งที่อุณหภูมิสูงกว่าเคลื่อนที่เร็วขึ้นทำให้สามารถชนกันได้บ่อยและมีประสิทธิภาพมากขึ้น
2. ขนาดของตัวถูกละลาย
ยิ่งเม็ดตัวถูกละลายมีขนาดเล็กก็จะละลายในตัวทำละลายได้ง่ายขึ้น เม็ดถูกละลายจำนวนน้อยทำให้พื้นที่ผิวของสารกว้างขึ้นและกระจายออกไปในสารละลาย
ยิ่งพื้นที่ผิวของสารมีขนาดใหญ่อนุภาคก็ชนกันมากขึ้น นี่คือสาเหตุที่ทำให้กระบวนการละลายเกิดเร็วขึ้น
3. ปริมาณตัวทำละลาย
ปริมาณมากของตัวทำละลายมีผลต่อกระบวนการละลายสาร ทั้งนี้เนื่องจากอนุภาคของตัวทำละลายทำปฏิกิริยากับตัวถูกละลายมากขึ้น
ยิ่งใช้ตัวทำละลายในปริมาตรมากเท่าไหร่กระบวนการละลายตัวถูกก็จะเร็วขึ้นเท่านั้น
4. ความเร็วในการผสม
กระบวนการละลายจะเร็วขึ้นหากคุณเพิ่มปัจจัยกวน
ด้วยการกวนอนุภาคของตัวถูกละลายจะถูกผสมกับตัวทำละลายมากขึ้นเพื่อให้ปฏิกิริยาการละลายเร็วกว่าการละลายโดยไม่ต้องกวน
นี่คือคำอธิบายเกี่ยวกับสารละลายและความสามารถในการละลายพร้อมกับความหมายคุณสมบัติประเภทและปัจจัย อาจมีประโยชน์.
